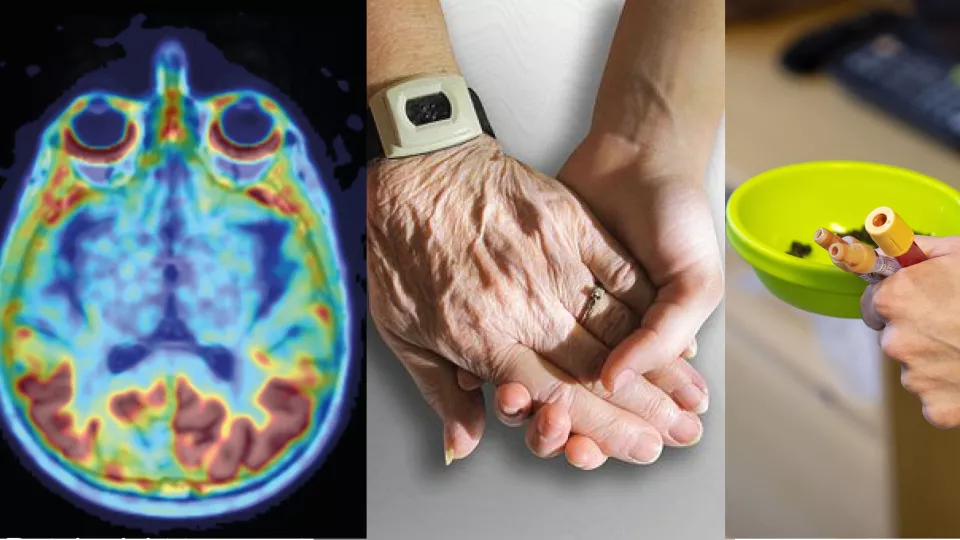
September är internationella Alzheimersmånaden. I Sverige räknas ungefär 100 000 lida av sjukdomen. Och antalet väntas öka i takt med vår åldrande befolkning. Tau och amyloid-beta är två proteiner som ansamlas och sprids i hjärnan hos personer med Alzheimers sjukdom. Trots att detta länge varit känt och att forskare arbetat intensivt med dyra kliniska prövningar saknas ännu botemedel. Ett problem är att de sjukliga förändringarna redan har pågått i årtionden innan patienterna blir så sjuka att de uppsöker vård och får sin diagnos. Då är skadorna stora och svåra att reparera. Men det senaste årets upptäckter och förbättrade diagnostiska verktyg från MultiParks forskargrupper inger nytt hopp.
Fyra olika typer av Alzheimer’s sjukdom
Professor Oskar Hansson, MultiParks vice koordinator, leder arbetet med de så kallade BioFINDER-studierna tillsammans med forskare vid Lunds universitet och Skånes universitetssjukhus. BioFINDER är en guldgruva för klinisk forskning på biomarkörer som på sikt ska kunna användas för tidig och säker diagnos av Alzheimer’s sjukdom. Studierna är unika i sitt slag, med sina över 3000 friska kontroller och patienter med Alzheimers eller andra neurodegenerativa sjukdomar. Tidigare i år gav undersökningar i BioFINDER upphov till inte mindre än två banbrytande upptäckter.
I april presenterades en internationell studie där BioFINDER ingick. Den visade att Alzheimers-proteinet tau sprids enligt fyra distinkta mönster. Varje spridningsmönster leder också till skilda symptom och olika prognoser för patienterna.
En algoritm förutspår Alzheimers
En månad senare, i maj, användes samma studie för att utveckla en algoritm som kombinerar resultatet från ett enkelt blodprov med snabba minnestester för att på individnivå förutspå vem som utvecklar Alzheimers sjukdom. Verktyget har över 90% träffsäkerhet. Blodprovet mäter en variant av tau-proteinet samt en riskgen för Alzheimers och det kognitive testet tar bara tio minuter att genomföra.
”Vi har nu utvecklat ett onlineverktyg för att beräkna risken på individnivå för att en person med lindriga minnessvårigheter kommer att utveckla alzheimer inom 4 års tid, berättar Sebastian Palmqvist, försteförfattare till studien och överläkare vid Minneskliniken, Skånes universitetssjukhus.
Tvärvetenskaplig samverkan för att förbättra vården för Alzheimerspatienter
Baserat på upptäckterna i BioFINDER har nio seniora forskare från fem olika fakulteter vid Lunds universitet initierat ett tvärvetenskapligt samarbete för att förbättra tidig diagnosticering av Alzheimers sjukdom. Fyra av dem är forskningsledare MultiPark, varav Oskar Hansson koordinerar samverkan. Andra medverkande är Region Skåne, Lunds kommun samt diagnostik- och läkemedelsindustrin.
”Under de senaste åren har vi haft stora genombrott när det gäller blodbaserade biomarkörer för Alzheimers sjukdom. Nu vill vi utveckla korrekta och kostnadseffektiva diagnostiska och prognostiska algoritmer som kan användas i både klinisk praxis och prövningar,” förklarar Oskar Hansson.
”Vi är mycket tacksamma för detta stöd; det gör det möjligt för oss att skapa en plattform för att generera gemensam kunskap och identifiera samarbetsprojekt,” tillägger Maria H Nilsson, vice koordinator för initiativet och en av forskningsledarna från hälsovetenskaper i MultiPark.
Enkla diagnosverktyg öppnar också nya möjligheter för läkemedelsutveckling, eftersom verktygen gör det lättare att rekrytera personer redan i ett tidigt stadium av Alzheimers då nya läkemedel har en bättre chans att bromsa sjukdomsutvecklingen. Men att finna nya lovande måltavlor där läkemedel kan påverka kräver större kunskap om tidiga sjukliga förändringar på molekylär nivå. Och häri finns MultiParks styrka som tvärvetenskaplig forskningsmiljö. I somras gjorde MultiParks experimentella forskare två viktiga upptäckter.
Amyloid-beta ansamlas tidigt inuti nervcellerna
I mitten av juli, medan de flesta svenskar höll semester, rapporterade forskare från den experimentella demensforskargruppen att amyloid-beta ansamlas inuti nervceller och att det felveckade proteinet därefter kan spridas mellan nervcellerna. Detta sker före amyloid-beta klumpar ihop till så kallade plack i hjärnan.
”Placken av amyloid-beta utanför nervcellerna har länge varit en måltavla för behandling vid Alzheimers sjukdom. Men då behandlingar för att ta bort plack inte har hjälpt mot demenssjukdomen måste vi utveckla och undersöka andra hypoteser för att på sikt finna andra måltavlor för behandling. Våra resultat pekar på att amyloid-beta är högst relevant men att vi måste fokusera på felveckat amyloid-beta inuti nervcellerna som uppkommer långt tidigare än de synliga placken,” säger försteförfattaren av studien Tomas Roos, doktorand i en av MultiParks forskargrupper och ST-läkare på neurologiska kliniken SUS Lund.
Att kunna observera strukturella förändringar hos molekyler som amyloid-beta kan alltså vara nyckeln till att förstå vad som går fel vid Alzheimers. Dessvärre har teknisk kunskap om hur processen ska kunna fångas på bild varit knapphändig.
Nya möjligheter att följa strukturella förändringar hos Alzheimers-proteiner inuti nervceller
En vecka senare, i slutet av juli, skulle en annan av MultiParks över 40 seniora forskare komma att presentera en lösning på problemet. Den medicinska mikrospektroskopi-gruppen visade då hur ett nytt tillvägagångssätt för avbildning kan ge information om struktur och kemisk sammansättning inuti en enskild nervcell.
”Med vår metod kartlägger vi fördelning av grundämnen och fibrillära former av amyloid-β-proteiner inom samma nervcell, med subcellulär upplösning,” förklarar Oxana Klementieva som leder gruppen Medical Microspectroscopy på MultiPark.
Hemligheten bakom att få så pass detaljerad information om strukturen är att kombinera redan etablerade tekniker i de båda ändarna av det elektromagnetiska spektrumet. Tillsammans blir de en perfekt kombination. Genom att använda röntgenstrålning kan metalljoner spåras ner till nanometersnivå. I andra delen av spektrumet kan infraröd strålning användas för att bedöma molekylära strukturer. Med dessa tekniker är det möjligt att spåra grundämnen och relevanta molekylära strukturer direkt i neuroner. Således höjer MultiParks pågående forskningsprojekt förväntningarna på att reda ut pusslet om Alzheimers sjukdom, en bit i taget.